衰老机制
为什么我们会衰老?
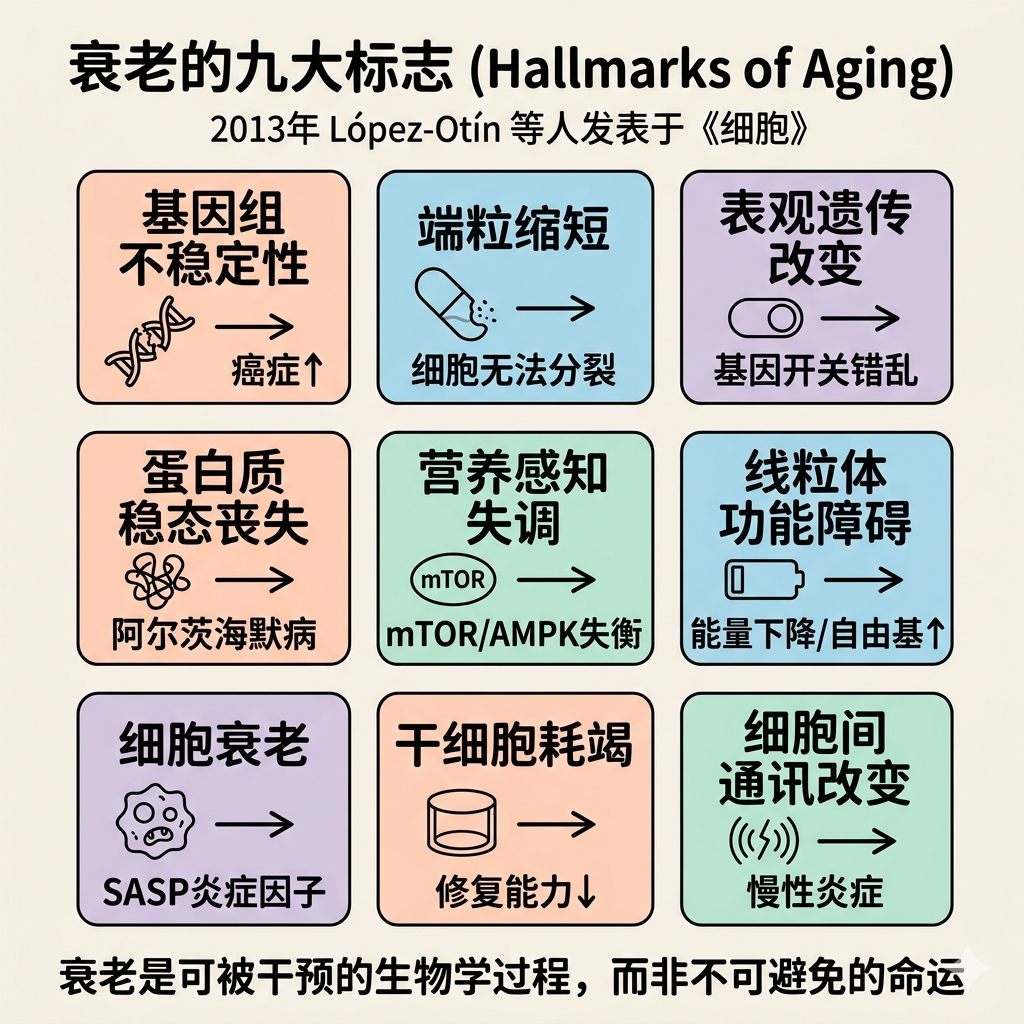
衰老不是一个单一的过程,而是多种细胞和分子损伤随时间积累的结果。2013年,科学家 López-Otín 等人在《细胞》杂志发表了”衰老的标志”(Hallmarks of Aging),总结了衰老的核心生物学特征。
核心观点
衰老是可以被干预的生物学过程,而非不可避免的命运。理解衰老机制,是找到干预点的前提。
衰老的九大标志(通俗版)
| 标志 | 通俗解释 | 与疾病的关联 |
|---|---|---|
| 基因组不稳定性 | DNA 损伤积累,修复能力下降 | 癌症风险增加 |
| 端粒缩短 | 染色体”保护帽”磨损,细胞无法继续分裂 | 细胞衰老、器官功能下降 |
| 表观遗传改变 | 基因”开关”错乱,该开的关了,该关的开了 | 多种慢性病 |
| 蛋白质稳态丧失 | 错误折叠蛋白质堆积,清除能力下降 | 阿尔茨海默病、帕金森病 |
| 营养感知失调 | mTOR/AMPK/IGF-1 通路失衡 | 代谢疾病、癌症 |
| 线粒体功能障碍 | 细胞”发电站”效率下降,产生更多自由基 | 肌肉无力、认知下降 |
| 细胞衰老 | 老化细胞不死亡,反而分泌炎症因子 | 慢性炎症、组织功能下降 |
| 干细胞耗竭 | 组织修复能力下降 | 伤口愈合慢、器官再生能力弱 |
| 细胞间通讯改变 | 细胞之间的”信号”紊乱,慢性炎症 | 几乎所有慢性病 |
重点机制详解
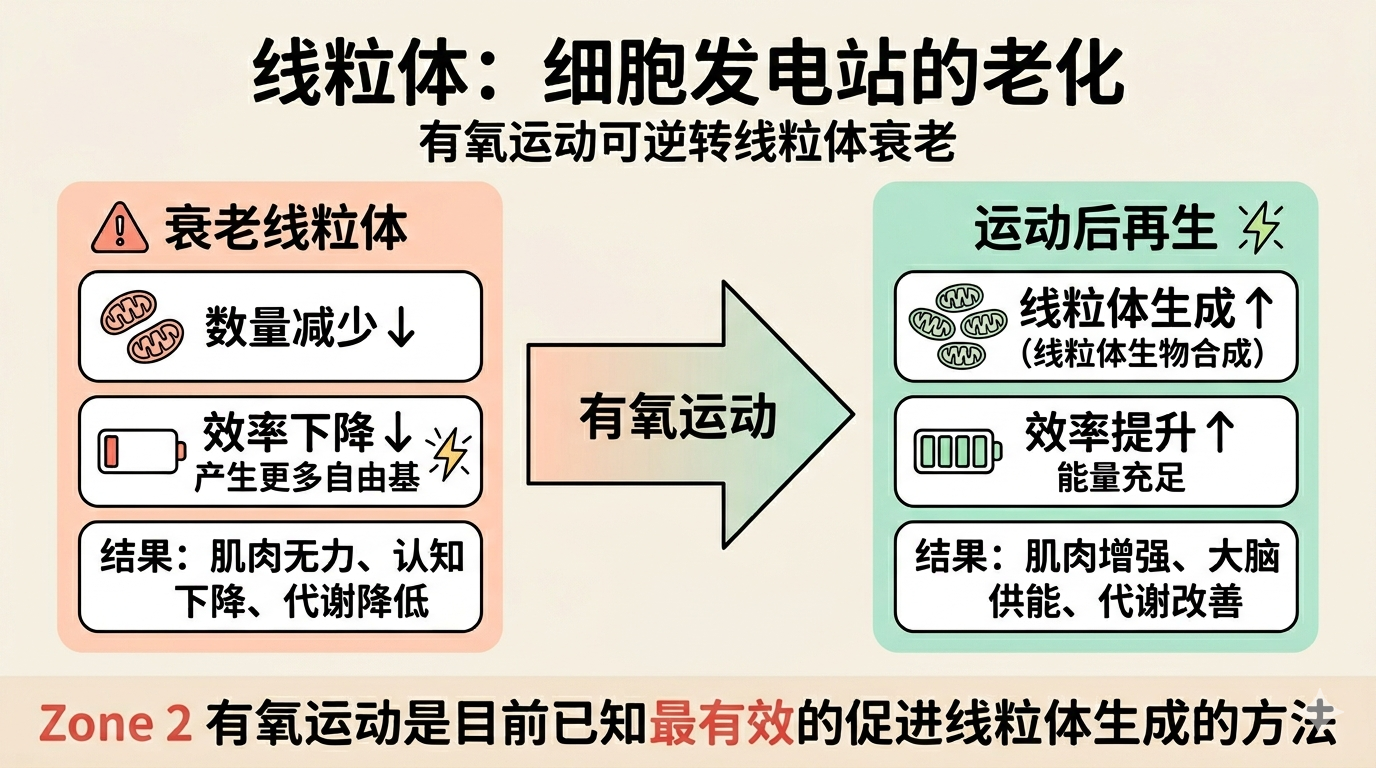
1. 线粒体功能障碍
线粒体是细胞的”发电站”,负责将食物转化为 ATP(细胞能量货币)。
随年龄发生的变化:
- 线粒体数量减少
- 线粒体效率下降
- 产生更多活性氧(自由基),损伤 DNA 和蛋白质
为什么重要:
- 肌肉力量下降(肌少症的原因之一)
- 大脑能量供应不足(认知下降)
- 代谢效率降低
好消息
有氧运动(尤其是 Zone 2 训练)是目前已知最有效的促进线粒体生成(线粒体生物合成)的方法。运动可以逆转线粒体老化。
2. 细胞衰老(Senescent Cells)
衰老细胞是那些停止分裂但拒绝死亡的细胞。它们会持续分泌炎症因子(称为 SASP),像”坏苹果”一样影响周围健康细胞。
正常细胞 → DNA 损伤 → 细胞衰老
↓
分泌炎症因子(SASP)
↓
周围组织慢性炎症 → 加速衰老
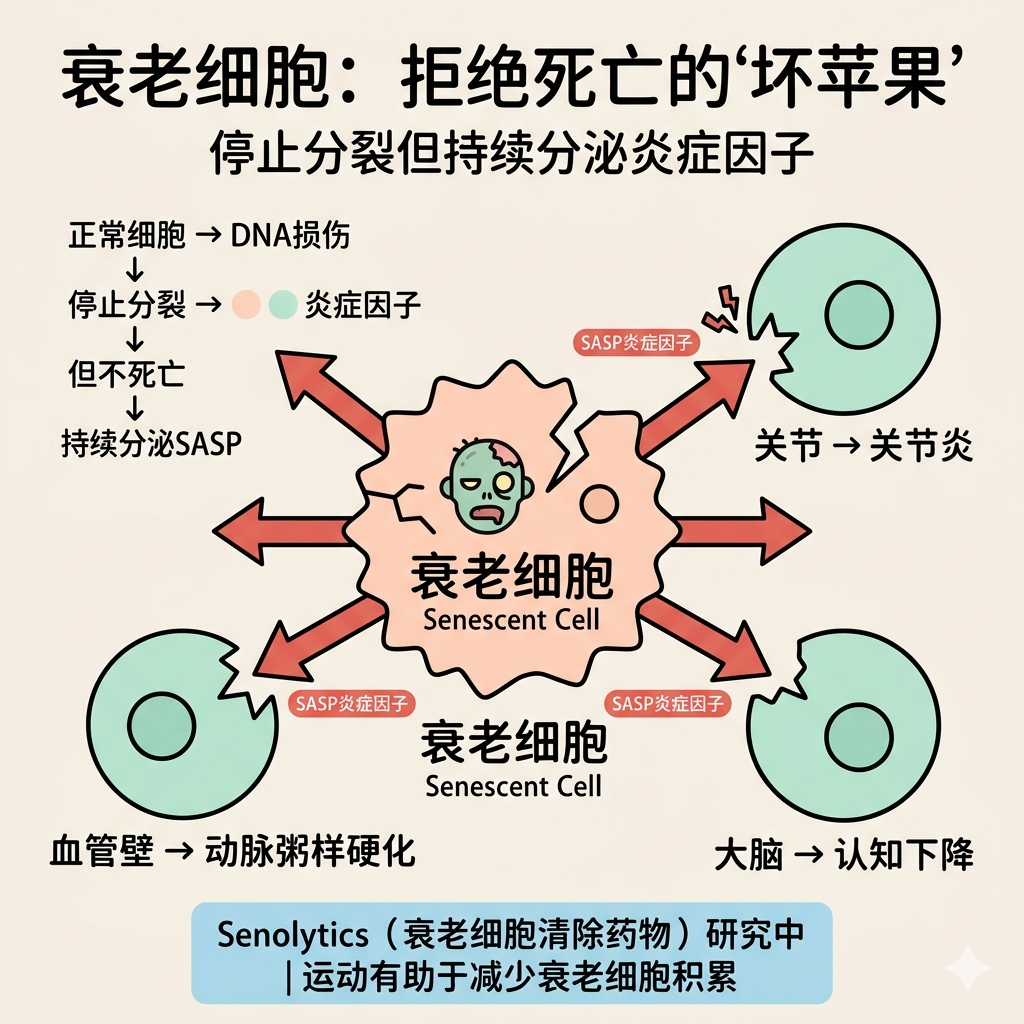
与疾病的关联:
- 关节炎(关节中衰老细胞积累)
- 动脉粥样硬化(血管壁衰老细胞)
- 认知下降(大脑中小胶质细胞衰老)
干预方向:
- Senolytics(衰老细胞清除药物):目前仍在研究阶段
- 运动:有助于减少衰老细胞积累
3. 端粒缩短
端粒是染色体末端的”保护帽”,每次细胞分裂都会缩短一点。
- 端粒过短 → 细胞停止分裂(进入衰老状态)
- 端粒酶可以延长端粒,但在大多数成体细胞中活性很低
端粒长度的局限性
市面上有”检测端粒长度”的商业服务,但彼得·阿提亚认为其预测价值有限——端粒长度受多种因素影响,单独测量意义不大。
4. 慢性炎症(Inflammaging)
“Inflammaging”= Inflammation(炎症)+ Aging(衰老),指随年龄增长出现的低度慢性炎症状态。
来源:
- 衰老细胞分泌的 SASP
- 肠道菌群失调
- 内脏脂肪(脂肪组织本身会分泌炎症因子)
- 睡眠不足
- 慢性压力
危害:
- 加速动脉粥样硬化
- 促进胰岛素抵抗
- 损伤神经元
- 促进癌症发展
衰老与四骑士的关系
衰老生物学变化
├── 线粒体功能障碍 → 代谢效率下降 → 胰岛素抵抗 → 2型糖尿病
├── 慢性炎症 → 血管损伤 → 动脉粥样硬化 → 心脏病
├── 蛋白质稳态丧失 → 错误蛋白堆积 → 阿尔茨海默病
└── 基因组不稳定 + 细胞增殖失控 → 癌症
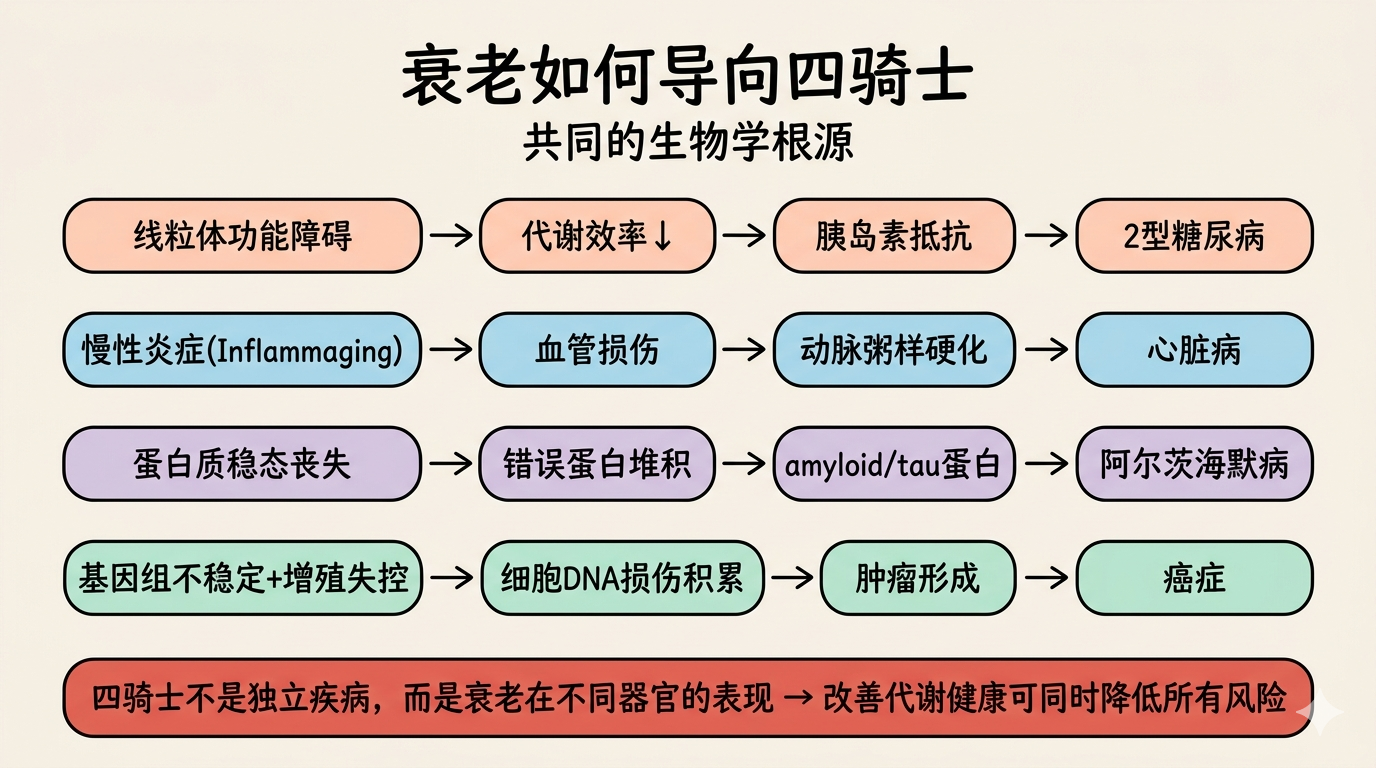
关键洞见
四骑士不是独立的疾病,而是衰老生物学变化在不同器官系统的表现。这就是为什么改善代谢健康可以同时降低所有四骑士的风险。
可以干预的衰老因素
| 干预方式 | 针对的衰老机制 | 证据强度 |
|---|---|---|
| 有氧运动(Zone 2) | 线粒体功能障碍 | 强 |
| 力量训练 | 肌少症、线粒体 | 强 |
| 热量限制 / 断食 | mTOR 过度激活、自噬不足 | 中等 |
| 睡眠优化 | 蛋白质清除(大脑淋巴系统) | 强 |
| 控制内脏脂肪 | 慢性炎症 | 强 |
| 压力管理 | 慢性炎症、端粒损耗 | 中等 |
相关笔记
- mTOR-AMPK-自噬通路 — 营养感知通路详解
- 百岁老人与长寿遗传 — 长寿基因如何对抗衰老
- 运动与长寿-总论 — 运动对衰老机制的干预
- 阿尔茨海默病预防 — 蛋白质稳态与神经退行性疾病
- 胰岛素抵抗 — 代谢衰老